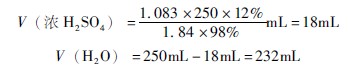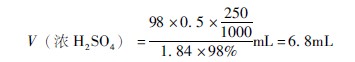535 化學(xué)溶液如何配制?作者:馬清浩 一、實驗?zāi)康?/span> (1)熟練掌握指定質(zhì)量分?jǐn)?shù)和指定濃度溶液的配制方法。 (2)練習(xí)溶液攪拌及藥品稱重的基本技能操作。 (3)掌握質(zhì)量濃度、物質(zhì)的量的濃度的計算方法。 二、實驗儀器設(shè)備 托盤天平;10mL,25mL,100mL,250mL量筒;250mL試劑瓶;250mL棕色試劑瓶;藥匙; 玻璃棒;滴管;標(biāo)簽;250mL燒杯。 三、實驗試劑與材料 NaCl(固體、化學(xué)純);濃硫酸(化學(xué)純);CuSO4·5H2O (固體、化學(xué)純)。 四、實驗內(nèi)容 (一)指定某質(zhì)量分?jǐn)?shù)溶液的配制 (1)配制200g質(zhì)量分?jǐn)?shù)為10%的NaCl溶液 ①計算配制200g質(zhì)量分?jǐn)?shù)為10%的NaCl溶液,所需NaCl和水的質(zhì)量。 稱取NaCl:200g×10% =20g 量取水:200mL-20mL=180mL ②用托盤天平稱出NaCl 20g,倒入250mL量筒,量取180mL蒸餾水,倒入盛有NaCl的燒杯內(nèi),用玻璃棒攪動,使NaCl全部溶解。 ③將配好的200g質(zhì)量分?jǐn)?shù)為10%的NaCl溶液沿玻璃棒注入250mL細(xì)口瓶中,蓋嚴(yán)瓶塞,貼好標(biāo)簽備用。 (2)用密度為1.84g/cm3、質(zhì)量分?jǐn)?shù)為98%的濃硫酸配制250mL密度為1.083g/cm3、質(zhì)量分?jǐn)?shù)為12%的稀H2SO4溶液 ①計算出配制250mL質(zhì)量分?jǐn)?shù)為12%的稀H2SO4溶液所需要的濃硫酸和水的體積
②用250mL量筒量取232mL蒸餾水,倒入250mL燒杯中,再用25mL量筒量取18mL濃硫酸,沿玻璃棒緩緩倒入上述燒杯中,邊倒邊攪拌,使其混合均勻并冷卻。 ③將配好并冷卻至室溫的硫酸溶液沿玻璃棒注入250mL試劑瓶中,蓋嚴(yán)瓶塞,貼好標(biāo)簽備用。 (二)指定物質(zhì)的量濃度(簡稱濃度)溶液的配制 (1)配制500mL 0.1mol/L的NaOH溶液 ①計算配制500mL 0.1mol/L的NaOH溶液所需固體NaOH的質(zhì)量 設(shè)500mL 0.1mol/L的NaOH溶液中含NaOH的質(zhì)量為X(g), 則 1000:500=4:X X=2g ②用拖盤天平稱取2g氫氧化鈉,放入潔凈的250mL燒杯中,加適量蒸餾水溶解,將溶液沿玻璃棒注入500mL試劑瓶中,并用少量蒸餾水洗滌燒杯2~3次,洗滌液也注入試劑瓶中,然后用蒸餾水將溶液稀釋至500mL,蓋緊瓶塞,搖勻后貼好標(biāo)簽備用。 (2)用密度為1.84g/cm3、質(zhì)量分?jǐn)?shù)為98%的濃H2SO4配制250mL 0.5mol/L的稀H2SO4溶液 ①計算配制250mL 0.5mol/L/的稀H2SO4溶液所需濃硫酸的體積
②往250mL干凈的燒杯中注入大約100mL蒸餾水,用10mL量筒量取濃H2SO4 6.8mL,沿玻璃棒緩緩注入燒杯內(nèi),并不斷攪拌,量筒用少量蒸餾水洗滌2次,洗滌液也注入燒杯中,用玻璃棒慢慢攪動,使溶液混合均勻并冷卻。 ③把冷卻至室溫的硫酸溶液沿玻璃棒注入250mL試劑瓶中,用少量蒸餾水洗滌燒杯、玻璃棒2~3次,洗滌液也注入試劑瓶中,然后用蒸餾水將溶液稀釋至250mL,搖勻后貼好標(biāo)簽備用。 |