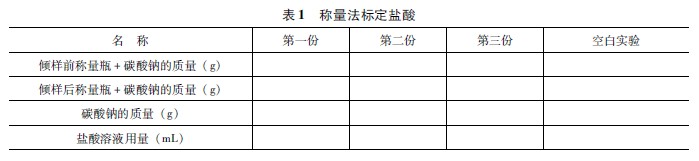
541 鹽酸溶液如何配制與標定?作者:馬清浩 一、實驗目的 (1)熟練掌握稱量和滴定操作。 (2)掌握用甲基橙、溴甲酚藍甲基紅作指示劑判斷滴定終點的方法。 (3)掌握用基準無水碳酸鈉標定鹽酸溶液的方法。 二、實驗原理 以甲基橙、溴甲酚藍甲基紅作指示劑,用鹽酸溶解滴定基準無水碳酸鈉,其反應為 Na2CO3+2HCl→2NaCl+H2O+CO2↑ 根據基準無水碳酸鈉的質量及所消耗鹽酸溶液的體積,即可計算出鹽酸溶液的基準濃度。 三、實驗儀器 分析天平;高溫爐;干燥器;坩堝鉗;1000mL燒杯1個;1000mL試劑瓶一個;250mL錐形瓶2個;50mL堿式滴定管1支。 四、實驗試劑 濃鹽酸;無水碳酸鈉(固體,基準試劑);質量分數為0.1%甲基橙指示液;溴甲酚綠甲基紅混合指示劑[質量分數為0.1%的溴甲酚綠酒精溶液與質量分數為0.2%的甲基紅酒精溶液以體積比(3+1)混合]。 五、實驗內容 (一)0.1mol/L鹽酸標準滴定溶液的配制 量取密度為1.19g/cm3的濃度酸9mL,注入1000mL盛有蒸餾水的燒杯中,搖勻后轉入試劑瓶中。 (二)0.1mol/L鹽酸標準滴定溶液的標定 (1)標定步驟用稱量瓶按遞減量法稱取在270~300℃灼燒至恒重的基準無水碳酸鈉0.15~0.2g(稱準至0.0002g),放入250mL錐形瓶中,以50mL蒸餾水溶解,加溴甲酚藍甲基紅混合指示劑10滴煮沸2min,冷卻后繼續滴定至溶液呈暗紅色為終點。平行測定三次,同時做空白實驗。將測定結果記錄于表1中。
(2)計算結果
式中m——無水碳酸鈉質量的準確數值,g; V1——鹽酸溶液體積的數值,mL; V0——空白試驗鹽酸溶液體積的數值,mL; M——無水碳酸鈉摩爾質量數值,M(1/2Na2CO3) =52.994g/mol。 取以上平行測定三次的算術平均值為測定結果,并按標準滴定溶液濃度的調整法,將測得的鹽酸溶液濃度調整到(0.1000±0.0005)mol/L。 |